- Heizmaterialien
Heizmaterialien (Heizstoffe, Brennmaterialien, Brennstoffe), Körper meist organischen Ursprungs, deren Beschaffungspreis die Anwendung zur Erzeugung von Wärme durch Verbrennung für gewerbliche und häusliche Zwecke gestattet. Die gebräuchlichsten H. sind: Holz, Torf, Braun-, Steinkohle, Anthrazit. Unter gewissen Verhältnissen kommen noch allerlei Abfälle, wie Gerberlohe, getrocknete Pflanzen, Stroh etc., hinzu. Alle diese H. bestehen im wesentlichen aus Kohlenstoff, Wasserstoff und Sauerstoff, und zwar wächst der Kohlenstoffgehalt in der angegebenen Reihenfolge vom Holz bis zum Anthrazit, während in demselben Maß der Sauerstoff- und der Wasserstoffgehalt abnehmen. Es enthalten
Als flüssiges Heizmaterial benutzt man Erdöl, das nur aus Kohlenstoff und Wasserstoff besteht, und in untergeordneter Weise Terpentinöl und fette Öle, als gasförmiges die brennbaren Gase, die an manchen Orten dem Erdboden entströmen und wesentlich auch aus Kohlenwasserstoffen bestehen. Neben diesen natürlichen werden künstliche H. benutzt: Holz- und Torfkohle und Steinkohlenkoks, Teer, Abfälle von der Destillation des Erdöls, Spiritus, seltener Methylalkohol, Glyzerin, in immer ausgedehnterm Maß aber Gase, die aus geringwertigen H. durch trockne Destillation dargestellt werden (Gasfeuerung); ferner Wassergas, Dowsongas, Leuchtgas, Gichtgase etc. Alle diese Heizgase bestehen im wesentlichen aus Kohlenoxyd, Kohlenwasserstoff und Wasserstoff.
Die hauptsächlichsten Bestandteile der H. sind also Kohlenstoff, Wasserstoff und Sauerstoff, und die Wärmeentwickelung beruht darauf, daß Kohlenstoff und Wasserstoff (auch der etwa vorhandene Schwefel) sich mit dem Sauerstoff der Luft verbinden, also verbrennen. Die letzten Verbrennungsprodukte bestehen aus Kohlensäure CO2 und Wasser H2O (das des Schwefels aus schwefliger Säure SO2). Werden Holz, Torf, Braunkohle, Steinkohle in Brand versetzt auf glühende Kohle geworfen, so entwickeln sie reichlich Dämpfe und Gase, die mit großer Flamme verbrennen, Anthrazit, Holzkohle, Koks entwickeln keine Dämpfe und Gase und verbrennen ohne Flamme. In beiden Fällen kann bei ungenügender Luftzufuhr unvollständige Verbrennung stattfinden, die Kohle kann zu Kohlenoxyd CO statt zu Kohlensäure verbrennen, Dämpfe und Gase können z. T. unverbrannt entweichen, die kohlenstoffreichern werden unter Ausscheidung von sein verteiltem Kohlenstoff (Ruß) zersetzt, die Verbrennung erfolgt unter Bildung von Rauch. Nach einiger Zeit hört die Entwickelung von Dämpfen und Gasen aus den zuerst genannten Brennmaterialien auf, und es hinterbleibt ein Rückstand, der fast nur aus Kohlenstoff besteht (»entgast ist«) und weiterhin ohne Flamme zu Kohlensäure (bez. Kohlenoxyd) verbrennt. Steinkohlen werden oft unter Abschluß der Luft erhitzt, die entweichenden Gase und Dämpfe anderweitig verwertet und die rückständigen Koks als Heizmaterial benutzt.
Der Wert der H. wird herabgemindert durch Gehalt an hygroskopischem Wasser (das behufs seiner Verdampfung einen Teil der erzeugten Wärme in Anspruch nimmt, aber durch Trocknen, Darren des Brennmaterials vor seiner Verwendung entfernt werden kann), an Schwefel, der wegen der Bildung von schwefliger Säure manche H. für gewisse Zwecke ganz unbrauchbar macht, endlich durch den Gehalt an mineralischen Stoffen, die bei der Verbrennung als Asche zurückbleiben. Die mineralischen Stoffe vermindern den Wert eines Heizmaterials, weil sie zur Wärmeentwickelung nichts beitragen, doch Raum beanspruchen und die Transportkosten erhöhen.
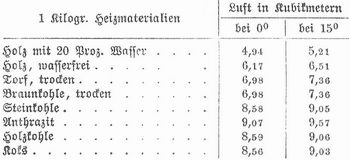
Der Gebrauchswert der H. richtet sich nach dem Zweck, den man mit ihnen erreichen will, und eine überall zutreffende Ordnung der H. nach ihrem Wert ist nicht zu geben. Für die einzelnen Fälle der Verwendung der H. berücksichtigt man die Brennbarkeit, die Flammbarkeit, hauptsächlich aber den zu erzielenden Wärmeeffekt. Die Brennbarkeit, d. h. die größere oder geringere Entzündlichkeit, ist abhängig von der physikalischen Beschaffenheit (Porosität) und der chemischen Zusammensetzung des Brennmaterials. Weiches Holz, besonders harzhaltiges, ist brennbarer als schweres, Holzkohle ist brennbarer als Koks und Steinkohle brennbarer als Anthrazit. Die Flammbarkeit, d. h. die Eigenschaft, mit mehr oder weniger großer Flamme zu verbrennen, ist, wie schon angedeutet, abhängig von der Entwickelung brennbarer Gase oder Dämpfe aus den erhitzten H. Leicht brennbarer H. bedarf man bei unvollkommenen Heizeinrichtungen, besonders bei solchen ohne Rost, wo schnelle Erwärmung auf nicht sehr hohe Temperatur erfolgen soll. Flammbare H. dienen zum unmittelbaren Erhitzen verhältnismäßig großer Räume oder großer Flächen, wie in Flammöfen und bei Kesselfeuerungen. Den größtmöglichen absoluten Wärmeeffekt erreicht man stets durch möglichst vollkommene Verbrennung des Brennmaterials und durch Vermeidung von Wärmeverlusten, wie sie z. B. durch Verdampfung von hygroskopischem Wasser herbeigeführt werden. Eine vollständige Verbrennung wird nur erreicht bei hinreichendem Luftzutritt. Die Kohlensäure, zu welcher der Kohlenstoff der H. verbrennt, enthält auf 1 Teil Kohlenstoff 2,66 Teile Sauerstoff. 100 Teile Luft enthalten aber nur 23,2 Teile Sauerstoff, also auf 1 Teil Sauerstoff 3,8 und auf 2,66 Teile Sauerstoff 8,78 Teile Stickstoff und andre für die Verbrennung nicht in Betracht kommende Bestandteile. 1 Teil Kohlenstoff braucht also, um zu Kohlensäure zu verbrennen, 11,44 Teile Luft und 1 kg Kohlenstoff, mithin 8,8 cbm. Ferner braucht 1 Teil Wasserstoff 8 Teile Sauerstoff, um zu Wasser zu verbrennen, also dreimal mehr als Kohlenstoff, demnach 34,32 Teile Luft, und 1 kg Wasserstoff mithin 26,1 cbm Luft. Hiernach brauchen zur vollständigen Verbrennung:
Erfahrungsgemäß reichen aber diese Luftmengen zur vollständigen Verbrennung nicht aus, sind vielmehr bis doppelt so groß zu nehmen, weil nur bei Überschuß von Sauerstoff sämtlicher Kohlenstoff zu Kohlensäure verbrennt. Dabei ist zu beachten, daß die Kohlensäure, wenn sie durch eine genügend starke Schicht glühender Kohle strömt, zu Kohlenoxyd reduziert wird. Auch soll bei der Verbrennung von Kohle in Luft unter 1000° viel Kohlensäure, bei höherer Temperatur überwiegend Kohlenoxyd entstehen.
Handelt es sich um Erzeugung möglichst hoher Temperaturen, so muß man die H. gut trocknen, um Wärmeverluste durch Verdampfung des hygroskopischen Wassers zu vermeiden; ferner müssen möglichst kompakte H. verwendet werden, um in demselben Raume mehr Brennstoff zu verbrennen. Man muß für energische Luftzuführung sorgen, um die Verbrennung zu beschleunigen, den Luftüberschuß aber möglichst beschränken und die Brennstoffe wie die Verbrennungsluft vorher erhitzen. Von der bei der Verbrennung entstehenden Gesamtwärme wird ein Teil zur Zerlegung der das Brennmaterial bildenden chemischen Verbindungen sowie zur Vergasung bei der Verbrennung entstehender Körper, also für innere Arbeit verwendet, der Rest tritt als freie Wärme in die Erscheinung. Diese nutzbare Wärme, bezogen auf die Gewichtseinheit des angewendeten Brennstoffes, heißt der absolute Wärmeeffekt (Heizeffekt, Brennkraft). Am vorteilhaftesten ist die Anwendung gasförmiger H., bei denen es allein möglich ist, das zur vollständigen Verbrennung erforderliche Luftquantum genau zu regulieren.
Der Temperaturgrad, den das Heizmaterial bei einer Anfangstemperatur von 0° und einem Druck von 760 mm entwickelt, heißt Heizkraft (pyrometrischer Heiz- oder Wärmeeffekt, Wärmeintensität). Heizkraft und Brennkraft zusammengenommen bestimmen den Wert eines Heizmaterials. Wird die Brennkraft auf den Wert des Heizmaterials bezogen, so erhält man dessen Brennwert. Das Produkt des absoluten Wärmeeffektes in das spezifische Gewicht eines Brennstoffes bildet den spezifischen Wärmeeffekt, die auf die Raumeinheit bezogene Verbrennungswärme. Bei der Verbrennung entsteht gleichviel Wärme, ob nun die Bildung der Endprodukte auf einmal oder in mehreren Phasen verläuft, d. h. ob die Bildung von Kohlensäure aus Kohlenstoff nach der Gleichung C+O2 = CO2 erfolgt, oder ob zunächst Kohlenoxyd gebildet wird C+O = CO und CO+O = CO2:
Dulong setzt voraus, daß der Wärmeeffekt eines zusammengesetzten Körpers gleich der Summe der Verbrennungswärme seiner Elementarbestandteile ist, daß bei sauerstoffhaltigen Körpern der Sauerstoff mit einem Teil des Wasserstoffes bereits zu Wasser verbunden ist und dieser Teil daher an der Wärmeentwickelung bei der Verbrennung nicht teilnimmt. Wenn also die Elementaranalyse einen Gehalt von C Proz. Kohlenstoff, H Proz. Wasserstoff und O Proz. Sauerstoff ergab, erhält man daraus die Verbrennungswärme des betreffenden Materials nach der Formel A = [8080C+34,500(H-O/8)]/100, wenn bei der Verbrennung der Wasserstoff des Materials in flüssiges Wasser, und A = [8080C+29,100(H-O/8)]/100, wenn er in Wasserdampf übergeführt wird. Die Richtigkeit der Voraussetzungen, unter denen die Dulongsche Formel aufgestellt wurde, ist vielfach bestritten worden, doch haben neuere Untersuchungen, wie die der Heizversuchsstation in München unter Verhältnissen, die denen der Praxis sehr nahe kamen, Heizwerte ergeben, welche die Brauchbarkeit der Dulongschen Formel für die Praxis erwiesen, und spätere Versuche von Schwackhöfer (1884) und von Bunte (1889–90) bestätigten diese Angaben. Nach den Vereinbarungen des internationalen Verbandes der Dampfkesselüberwachungsvereine und des Vereins deutscher Ingenieure lautet nunmehr die Dulongsche Formel (Verbandsformel): A = [8080C+29,000(H-O/8)+2500S-600W]/100, gibt den theoretischen Verdampfungseffekt, d. h. die Gewichtsmenge von Wasser von 0° an, die durch 1 Gewichtsteil des Brennstoffes in Dampf von 100° übergeführt werden kann. Dabei liegt die Annahme zugrunde, daß die Verbrennung ohne Luftüberschuß vor sich geht und die Verbrennungsprodukte, auf 0° abgekühlt, entweichen. In der Praxis rechnet man auf die Erreichung eines Verdampfungseffekts, der 3/5-2/3, bei guter Gasfeuerung 5/6 des theoretischen beträgt.
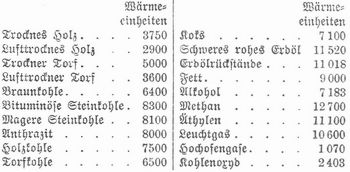
Die Heizkraft der Brennstoffe wird mit Hilfe des Kalorimeters bestimmt, sie beträgt:
Der pyrometrische Wärmeeffekt eines Heizmaterials kann ermittelt werden, indem man die Gewichtsmengen sämtlicher bei der Verbrennung auftretender Produkte mit der zugehörigen spezifischen Wärme (Luft 0,238, Wasserdampf 0,475, Kohlensäure 0,216, Kohlenoxyd 0,2479, Stickstoff 0,244, Asche 0,2) multipliziert und den ermittelten absoluten Wärmeeffekt durch die Summe dieser Produkte dividiert. In reinem Sauerstoff verbrannt, gibt 1 g Kohlenstoff 3,67 g Kohlensäure, und der pyrometrische Wärmeeffekt ist daher 8080/(3,67×0,216) = 10,187°. In der Luft verbrannt, kommen noch 8,88 g Stickstoff, mit dem der Sauerstoff verdünnt ist, in Rechnung, und die Verbrennungstemperatur ergibt daher 8080/(3,67×0,216+8,88×0,244) = 2731°. Da nun in der Praxis doppelt soviel Luft erforderlich ist, als die Rechnung ergibt, so sind auch noch 11,55 g Luft zu berücksichtigen, und man erhält
8080/(3,67×0,216+8,88×0,244+11,55×0,238) = 1415° als Ausdruck für den pyrometrischen Wärmeeffekt des Kohlenstoffes. In solcher Weise findet man, daß folgende Temperaturen erzielt werden können bei:
Führt man aber nur die einfache Luftmenge in den Verbrennungsraum ein, so daß die Hälfte des Kohlenstoffes zu Kohlensäure, die andre Hälfte zu Kohlenoxyd verbrannt wird, so erhält man folgende höhere Temperaturen:
Dies sind die höchsten Temperaturen, die sich technisch durch einfache Verbrennung der H. auf einem Rost in dem Feuerraum erreichen lassen. Bei Anwendung von Gasen aber und unter den oben angegebenen Bedingungen kann man dem theoretischen pyrometrischen Wärmeeffekt erheblich näher kommen.
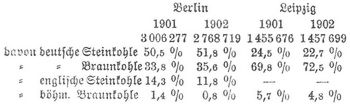
Statistisches. Der jährliche Zuwachs an Holz in den Wäldern Deutschlands beträgt etwa 40 Mill. Ton., wovon etwa 30 Mill. früher oder später §ur Verbrennung kommen. Der Brennwert dieses Holzes entspricht etwa 12 Mill. Ton. Steinkohle. Deutschland besitzt auch große Torflager, und in weiten Gebieten ist Torf ein wichtiges, ja das wichtigste Brennmaterial, immerhin hat er nur lokale Bedeutung, da er seiner Minderwertigkeit halber lange Fracht nicht verträgt. Über die Größe der Torfgewinnung fehlt jede brauchbare Angabe; seine Verwendung für die Industrie (Dampfkesselfeuerung, Gasfeuerung etc.) ist gering. An Mineralkohlen wurden in Deutschland (in Tonnen) gewonnen:
Der Verbrauch betrug:
Der Verbrauch an Steinkohlen im J. 1897 auf den Kopf der Bevölkerung betrug dagegen in Rußland 90, in Österreich-Ungarn 370, in Frankreich 980, in Deutschland 1580, in den Vereinigten Staaten 2450, in Belgien 2700, in England 3930 kg. Der Verbrauch an Stein- und Braunkohlen betrug (in Tonnen) in:
Vgl. Péclet, Traité de la chaleur (3. Aufl., Par. 1861, 3 Bde.); Fischer, Chemische Technologie der Brennstoffe (Braunschw. 1880–1901, Bd. 1 u. 2) und Die Brennstoffe Deutschlands etc. und die Kohlennot (das. 1901); Krüger, Lehre von den Brennmaterialien (Jena 1883); Bunte, Zur Wertbestimmung der Kohle (Verhandlungen der 30. Jahresversammlung des Vereins von Gas- und Wasserfachmännern); Fritzsche, Untersuchung und Bewertung der Brennstoffe (Leipz. 1897); Jüptner v. Jonstorff, Die Bestimmung des Heizwertes von Brennmaterialien (Stuttg. 1898); »Zusammenstellung der vergleichenden Versuche über die Heizkraft und andre in technischer Beziehung wichtige Eigenschaften verschiedener Steinkohlen, Preßkohlen und Koks. Ausgeführt auf den kaiserlichen Werften zu Wilhelmshaven, Kiel und Danzig von 1874–1894« (Berl. 1895).
http://www.zeno.org/Meyers-1905. 1905–1909.