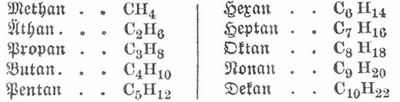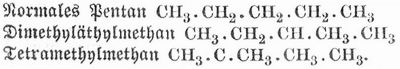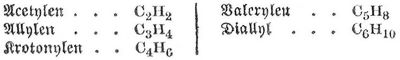- Kohlenwasserstoffe
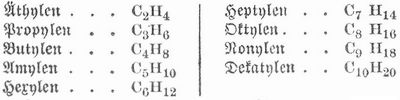
Kohlenwasserstoffe, chem. Verbindungen von Kohlenstoff mit Wasserstoff. Beide Elemente verbinden sich nur unter dem Einfluß starker elektrischer Entladungen direkt miteinander zu Acetylen, aber sie bilden so viele Verbindungen wie kein andres Paar von Elementen. Nach den Ergebnissen der Spektralanalyse bestehen die Kometen zum Teil aus Kohlenwasserstoffen, Pflanzen bilden K. als Hauptbestandteile der ätherischen Öle, als Kautschuk etc., sehr allgemein entstehen K. als Zersetzungsprodukte organischer Substanzen bei Fäulnis und Verwesung, gasförmige K. entströmen dem Boden. Das Erdöl besteht aus flüssigen, Ozokerit und ähnliche Mineralien aus festen Kohlenwasserstoffen. K. bilden sich auch bei der trocknen Destillation organischer Substanzen und finden sich daher im Leuchtgas und im Teer. Die große Anzahl der existierenden K. erklärt sich aus der Eigenschaft des Kohlenstoffs, durch Aneinanderlagerung und chemische Bindung seiner Atome Moleküle mit mehreren, ja mit vielen Kohlenstoffatomen zu bilden. Nach Art der Verkettung der Kohlenstoffatome unterscheidet man zwei große Gruppen von Kohlenwasserstoffen, die der Fettreihe und die der karbo- oder isozyklischen Reihe. Zu der Fettreihe gehören a) Gesättigte K. (Grenzkohlenwasserstoffe, Paraffine)von der Formel CnH2n+2. Diese K. leiten sich vom Methan CH4 ab und entstehen, indem an die Stelle von H-Atomen Methylgruppen CH3 treten. Aus CH4 wird CH3.CH3=C2H6 Äthan. aus diesem Propan CH3.CH2.CH3=C3H8 und CH3.CH2.CH2.CH3=C4H10 etc. Diese Methanreihe enthält als Anfangsglieder folgende homologe K.:
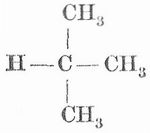
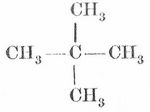
Aus dem Propan CH3.CH2.CH3 kann ein dem Butan isomerer Kohlenwasserstoff entstehen, indem das Wasserstoffatom der Gruppe CH2 durch CH3 ersetzt wird, nämlich das Trimethylmethan CH3.CH.CH3.CH3. Wird in letzterm Kohlenwasserstoff das Wasserstoffatom der Gruppe CH durch CH3 ersetzt, so entsteht Tetramethylmethan CH3.C.CH3.CH3.CH3, das mit Pentan isomer, aber strukturverschieden ist. Zum Unterschied von den primären Kohlenwasserstoffen, wie Propan, Butan, Pentan, deren C-Atome in einer offenen Kette angeordnet sind, nennt man die K. mit der Bindung des Trimethylmethans sekundäre und die mit der Bindung des Tetramethylmethans tertiär e.
Die Anzahl der Isomeren wächst mit der der im Molekül enthaltenen Kohlenstoffatome. Da im Methan alle vier Wasserstoffatome gleichwertig sind, so kann es nur ein Methan geben; es ist gleichgültig, welches Wasserstoffatom durch CH3 ersetzt wird, und mithin kann es auch nur ein Äthan geben. Ebenso kann aus letzterm nur ein Propan abgeleitet werden. Im Propan aber kann die Gruppe CH3 in die Gruppe CH2 oder in eine der beiden gleichwertigen Gruppen CH3 eintreten, und daher gibt es zwei Butane. Für das Pentan sind schon drei Isomere möglich:
Beim Hexan existieren 5, beim Heptan 9, beim Oktan 18 Isomere.
Bei den Grenzkohlenwasserstoffen sind alle Kohlenstoffatome untereinander nur durch eine Valenz verbunden, und die übrigen Valenzen sind durch Wasserstoff gebunden, die K. sind gesättigt. Ihnen gegenüber stehen die ungesättigten K., in deren Molekül zwei oder mehr Kohlenstoffatome mit mehr als einer Valenz verbunden sind. Hierher gehören die Äthylene (Olefine, Alkylene)CnH2n, deren erste Glieder sind:
Diese K. enthalten eine doppelte Bildung. z. B. Äthylen CH2=CH2, Propylen CH3.CH=CH2, Butylen CH3.CH2.CH=CH2. Sie addieren leicht zwei Halogenatome und gehen dadurch in gesättigte Verbindungen über. Eine andre Reihe ungesättigter K. bilden die Acetylene CnH2n-2, zu welchen
gehören. Sie enthalten eine dreiwertige Bindung: Allylen CH3.C≡CH, Krotonylen CH3.CH2.C≡CH. Noch wasserstoffärmere Reihen bilden die K. CnH2n-4 und CnH2n-6.
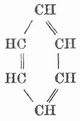
Während in den Kohlenwasserstoffen der Fettreihe die Kohlenstoffatome stets in offenen Reihen oder Ketten angeordnet sind, zeigen die karbo- oder isozyklischen K. einen andern Typus. Bei den wichtigsten dieser K., den aromatischen, deren Muttersubstanz das Benzol C6H6 ist, sind 6 Kohlenstoffatome mit
abwechselnd einfacher und doppelter Bindung zu einem Ring vereinigt, und indem nun an die Stelle von Wasserstoffatomen CH3-Gruppen treten, entstehen andre K. und viele Isomere (Ortho-, Meta-, Paraverbindungen, s. Aromatische Körper). Ferner können zwei oder mehrere einwertige Benzolreste (Phenyl) C6H5 durch gleichwertige Kohlenwasserstoffreste der Fettreihe verbunden werden, z. B. Diphenylmethan C6H5-CH2-C6H5 oder
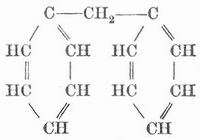
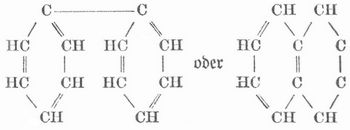
es können zwei Benzolkerne direkt durch je ein oder zwei Kohlenstoffatome in verschiedener Weise zusammenhängen, z. B.:
es können die verschiedenen Verkettungsweisen bei Einem Kohlenwasserstoff gleichzeitig auftreten, und überall können die Wasserstoffatome durch Kohlenwasserstoffreste der Fettreihe substituiert werden. So entsteht eine ungemein große Zahl von aromatischen Kohlenwasserstoffen mit zum Teil überaus komplizierter Struktur.
Die K. sind als die Muttersubstanzen aller organischen Verbindungen aufzufassen, die aus jenen durch Substitution von Wasserstoffatomen durch gleichwertige Atome oder Atomgruppen entstehen. Die Mehrzahl der K. läßt sich auf künstlichem Weg erhalten. Die K. mit einer geringen Anzahl von Kohlenstoffatomen sind Gase, die kohlenstoffreichern sind farblose, charakteristisch riechende, in Wasser nicht lösliche und spezifisch leichtere Flüssigkeiten, deren Siedepunkt mit dem Kohlenstoffgehalt steigt. Die kohlenstoffreichsten K. sind starre kristallisierbare Körper, deren Schmelzpunkt gleichfalls mit dem Kohlenstoffgehalt steigt. Die K. der Fettreihe, und besonders die gesättigten, sind wenig reaktionsfähig und sehr beständig (daher der Name Paraffine). In der Kälte werden sie von rauchender Salpetersäure und Chromsäure kaum angegriffen, in der Wärme aber meist vollständig zu Kohlensäure und Wasser verbrannt. Nur bei Einwirkung von Chlor und Brom bilden sie Substitutionsprodukte. Die ungesättigten K. vermögen noch Atome und Atomgruppen zu binden und sind deshalb reaktionsfähiger. Die Reaktionsfähigkeit der aromatischen K. ist am größten, sie bilden leicht Chlor-, Brom-, Nitrosubstitutionsprodukte und Sulfokörper und sind zur Bildung von Derivaten geeignet, die in der Fettreihe keine Analoga finden. Zahlreiche K. werden in der Technik benutzt.
http://www.zeno.org/Meyers-1905. 1905–1909.