- Soda
Zur Darstellung von Soda nach dem Leblancschen Prozeß wird zunächst Kochsalz oder Steinsalz (Chlornatrium) durch Schwefelsäure in schwefelsaures Natron (Sulfat) verwandelt. Hierbei entweicht Chlorwasserstoffgas, das in geeigneten Apparaten von Wasser aufgenommen wird. Diese Lösung bildet die Salzsäure. Die Zersetzung des Chlornatriums durch Schwefelsäure verläuft in zwei Stadien. Erhitzt man 2 Moleküle Chlornatrium mit 1 Molekül Schwefelsäure, so tritt lebhafte Reaktion ein, aber der Prozeß gelangt zum Stillstand, wenn 1 Molekül Chlornatrium in saures schwefelsaures Natron verwandelt ist. Man muß dann stärker erhitzen, damit das saure schwefelsaure Natron das zweite Molekül Chlornatrium zersetzt. Diesem Vorgang entsprechend sind die Sulfatöfen konstruiert. Sie enthalten eine eiserne Pfanne, in der die erste Phase des Prozesses verläuft, und aus der die Masse in einen andern Teil des Ofens, den Kalzinierraum, geschafft wird, um hier stärker erhitzt zu werden. Man benutzt aber zwei Formen von Öfen, Flammöfen, in denen das Arbeitsgut in direkte Berührung mit den Feuergasen kommt, so daß sich der entwickelte Chlorwasserstoff mit letztern mischt, und Muffelöfen, bei denen die Beschickung in einer von oben und von unten durch die Flamme bestrichenen Muffel erhitzt wird und der Chlorwasserstoff ohne fremde Beimengungen entweicht, so daß er leichter zu einer starken Säure kondensiert werden kann. Der Flammofen ist dagegen leistungsfähiger, muß aber mit Koks geheizt werden, damit die ohnehin schwierige Kondensation des mit den Feuergasen gemischten Chlorwasserstoffs nicht noch weiter durch Ruß erschwert wird.
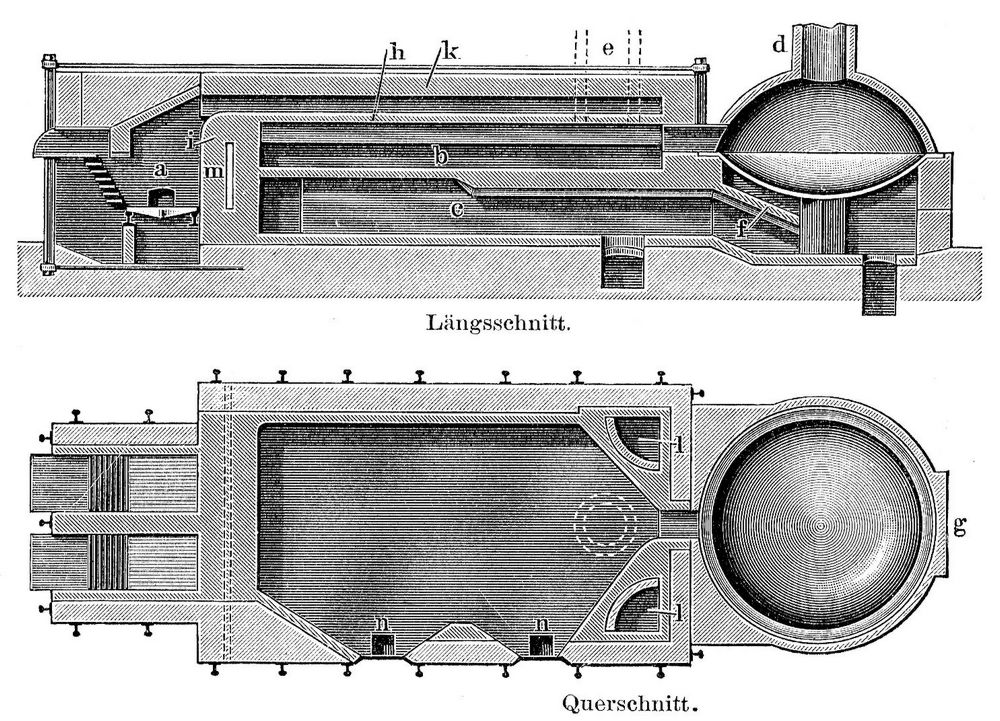 1 u 2. Sulfatofen.
1 u 2. Sulfatofen.Fig. 1 und 2 zeigen einen Sulfatofen. Die Feuergase gehen von der Feuerung a über die Feuerbrücke i und am Gewölbe h der Muffel b unter dem Obergewölbe k entlang und fallen dann durch die Kanäle 1 unter die Sohle der Muffel. Hier ziehen sie durch Kanäle c nach vorn und kommen durch innere Kanäle unter die Schale, umspülen diese und fallen in den Fuchs. Die Feuerbrücke wird durch den Schlitz m gekühlt, die Pfanne aber durch das Gewölbe f geschützt. g ist das Loch zum Füllen der Schale mit Salz, im Gewölbe der Schale befindet sich ein Trichterrohr zum Einfüllen der Schwefelsäure, n, n sind Arbeitslöcher. Das Chlorwasserstoffgas wird getrennt aus Schale und Herd abgeführt durch die Öffnungen d und e. Bei den mechanischen Sulfatöfen wird die ganze Operation in einer flachen, ausschließlich von oben geheizten gußeisernen Schale ausgeführt und durch einen Rührapparat sehr gefördert. Infolge der erzielten innigern Mischung gelangt man mit weniger Schwefelsäure und bei niedrigerer Temperatur zum Ziel, und die im regelmäßigem Strom entweichende Salzsäure ist, obwohl mit Feuerungsgasen gemischt, leichter kondensierbar. In den Pfannen der Sulfatöfen zersetzt man Chargen von 250–800 kg Kochsalz mit Schwefelsäure von 59–60° B. Die zähteigig gewordene Masse schafft man nach dem Kalzinierraum und erhitzt sie hier bis zu ziemlich heller Glut, und bis sich keine Dämpfe mehr entwickeln. 100 kg Siedesalz mit 6–8 Proz. Feuchtigkeit liefern 110 kg Sulfat.
Nach dem Verfahren der Sulfatbereitung von Hargreaves beschickt man 8–20 untereinander durch Röhren verbundene gußeiserne Zylinder mit Kochsalz in Form von plattenförmigen porösen Stücken und leitet durch Rösten von Schwefelkies erhaltene, mit Luft und überhitztem Wasserdampf gemischte Schweflige Säure hinein, während die Zylinder auf 500–550° erhitzt werden, bei welcher Temperatur der Inhalt sich vollständig in Sulfat verwandelt, während Salzsäuredämpfe entweichen. Die Schweflige Säure durchströmt einen Zylinder nach dem andern, die in derselben Reihenfolge fertig und neu beschickt werden. Zur Hervorbringung des erforderlichen Zuges in den Zersetzungsgefäßen und dem Pyritofen ist ein Gebläse am Ende des Apparats aufgestellt, der die aus Stickstoff, Chlorwasserstoff, überschüssiger Luft und etwas Schwefliger Säure bestehenden Endgase nach der Kondensation schafft. Bei diesem Verfahren wird also die Schwefelsäurefabrikation vollständig erspart, und die Kondensation des sehr gleichmäßig sich entwickelnden Chlorwasserstoffs macht keine Schwierigkeiten.
Das Sulfat besteht aus 95–98 Proz. schwefelsaurem Natron und enthält geringe Mengen Chlornatrium, Schwefelsäure, schwefelsaures Eisenoxydul etc. Um es in Soda zu verwandeln, schmelzt man 100 Teile mit 90–120 Teilen grob gepulvertem Kalkstein oder Kreide und 40–80 Teile Steinkohle im Flammofen. Dieser hat stets zwei Arbeitssohlen (Herde), von denen die eine, von der Feuerbrücke entferntere etwas höher liegt. Die Herde sind verhältnismäßig klein und nur auf eine Beschickung von ca. 400 kg eingerichtet.
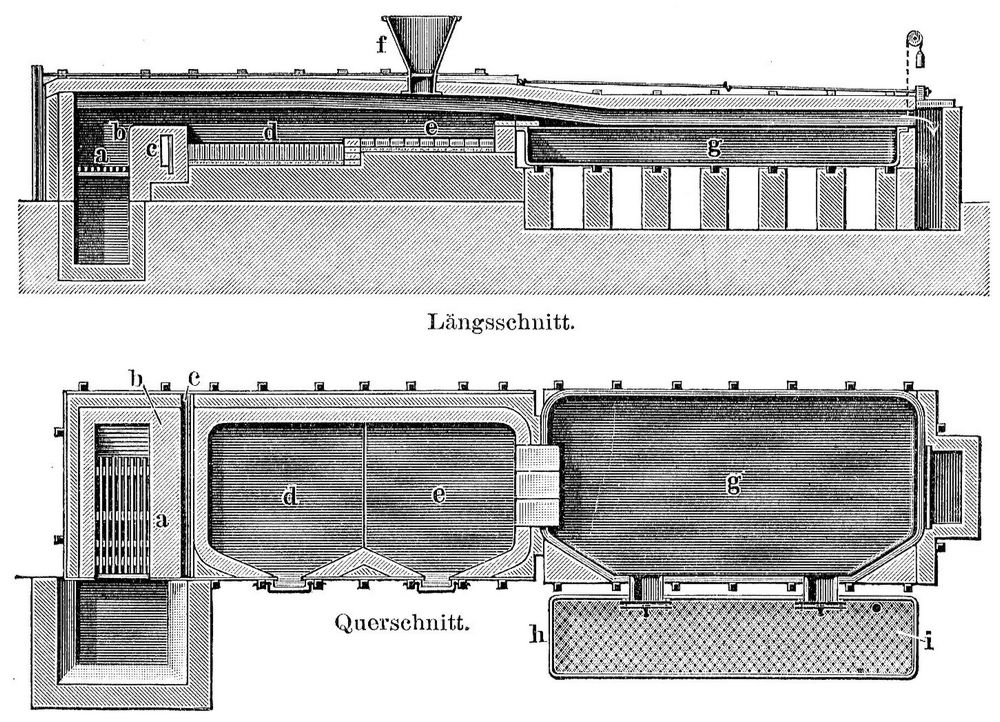 3 u. 4. Sodaofen.
3 u. 4. Sodaofen.In dem Sodaofen (Fig. 3 u. 4) ist a der Feuerraum mit den Rosten, b die hohle Feuerbrücke mit dem Luftkanal c; die Beschickung wird durch den Füllrumpf f auf den Herd e gebracht, von dem sie später nach d gelangt. Jeder Herd besitzt eine Arbeitstür mit abbalancierter Verschlußplatte. An den Ofen schließt sich eine Verdampfpfanne g an, die durch Oberfeuer geheizt wird. Sie besitzt zwei oder mehr Arbeitstüren zum Ausräumen, und vor denselben steht das Salzfilter h mit Siebboden i. In einer Aussackung des Filters steht die Mutterlaugenpumpe. Die Beschickung wird 40–50 Minuten auf dem Herd e vorgewärmt, dann in etwa gleicher Zeit auf dem Herde d zu ziemlich heftiger Weißglut gebracht und fleißig durchgearbeitet. Zuerst entwickelt sich aus der Masse Kohlensäure, dann brechen Kohlenoxydflammen hervor, und sobald diese reichlicher auftreten und die Masse steifer geworden ist, wird sie in eiserne Wagen gezogen und nach dem Erstarren aus diesen herausgestürzt. Die erhaltenen Brote (Bälle) bilden die Rohsoda. Auf 100 kg Sulfat werden 50–70 kg Kohle in der Feuerung verbrannt.
Große Vorteile gewähren die rotierenden Sodaöfen (Revolver), welche die Bewältigung größerer Massen gestatten und eine vollständigere Zersetzung des Sulfats sichern. Man wendet im rotierenden Ofen auf 100 Teile Sulfat 102 Teile Kalkstein in walnußgroßen Stücken und 45 Teile magere Kohle an. Im letzten Stadium des Sodaprozesses bilden sich Cyanverbindungen, die durch Zugabe von 6–7 Proz. Sulfat zersetzt werden, indem sich Schwefelnatrium, kohlensaures Natron, Kohlenoxyd und Stickstoff bilden (Na2SO4 + 2NaCN = Na2S + Na2CO3 + CO + 2N). Setzt man gleichzeitig kohlensauren Kalk hinzu, so wird das Natron vollständig in kohlensaures Natron übergeführt (Pechiney und Weldon). Einen rotierenden Ofen zeigt Fig. 5. Ein rotierender Ofen leistet soviel wie 3–4 Handöfen. Die gewöhnlichen Drehöfen sind 5 m lang und haben 3 m Durchmesser; man macht täglich 10–15 Operationen von je 1500 kg Sulfat. Man baut indes auch Revolver von 9 m Länge, die in der Woche 400 Ton. Sulfat verarbeiten.
Der rotierende Ofen (Revolver) ist ein liegender Zylinder aus Kesselblech, innen mit feuerfesten Steinen gefüttert und mit zwei Längsrippen versehen zur bessern Mischung der Beschickung beim Drehen. Eine Öffnung c dient zum Füllen und Entleeren. Die Heizung erfolgt durch Feuergase, die aus der Feuerung d durch eine Öffnung in der Stirnwand in den Zylinder gelangen und bei e austreten, um später Verdampfpfannen zu heizen. Der Zylinder dreht sich auf zwei ringförmigen Bändern a und b, die auf Friktionsscheiben f, f laufen, und wird mittels des Zahnrades g durch die Dampfmaschine h in Bewegung gesetzt. Anfangs macht der Revolver eine Drehung in 20, später in 1 Minute. Sobald die Masse ruhig fließt und am Ausgangspunkt des Revolvers die gelbe Natronflamme erscheint, wird die Schmelze in auf Schienen laufende Wagen abgelassen.
Die erhaltene Rohsoda bildet eine blasige, schlackenartige, steinharte, blaugraue Masse mit eingesprengten Koksstückchen und ist im wesentlichen ein Gemenge aus 36–45 Proz. kohlensaurem Natron, ca. 30 Proz. Schwefelcalcium, 5 Proz. Kalk, 7 Proz. Kohle, 3 Proz. Kieselsäure etc. Man kann annehmen, daß bei dem Sodabildungsprozeß das schwefelsaure Natron durch die Kohle unter Bildung von Kohlensäure zu Schwefelnatrium reduziert wird. Das schmelzende Schwefelnatrium bildet dann mit kohlensaurem Kalk Schwefelcalcium und kohlensaures Natron. Steigert sich nun die Temperatur, so wird noch vorhandener kohlensaurer Kalk durch Kohle unter Bildung von Kohlenoxyd in Ätzkalk (CaO) verwandelt. Die Rohsoda enthält auch Reste von unzersetztem Sulfat, Chlornatrium und kohlensaurem Kalk, Verunreinigungen der Rohmaterialien, wie Kieselsäure, Tonerde, Magnesia etc., dann auch Cyan- und Schwefelcyanverbindungen, Ammoniakverbindungen, Schwefeleisen, Schwefelnatrium, unterschwefligsaures Natron etc. Sie zieht an der Luft Feuchtigkeit an und wird rissig, indem der vorhandene Kalk sich löscht. Bei längerm Liegen an der Luft zerfällt die Rohsoda zu Pulver; es bilden sich Calciumsulfhydrat und aus diesem schwefelsaurer Kalk. Man läßt deshalb die Rohsoda nur zwei Tage an der Luft liegen, zerschlägt sie in handliche Stücke und laugt sie kalt in solcher Weise aus, daß man möglichst konzentrierte Laugen erhält.
Das Auslaugen geschieht systematisch in einer Reihe von Kasten, das Wasser tritt stets zunächst in einen Kasten mit schon fast vollständig erschöpfter, zuletzt aber in einen Kasten mit ganz frischer Masse, um sich möglichst vollständig zu sättigen. Der völlig erschöpfte erste Kasten wird neu beschickt und reiht sich nun dem letzten an, während das Wasser zunächst in den zweiten Kasten tritt, bis auch dieser erschöpft ist, etc. Eine Dampfleitung gestattet, die Lauge auf etwa 40° zu erwärmen. Aus dem letzten Kasten fließt Lauge von 27° B. ab. Beim Auslaugen wirken die Calciumverbindungen auf kohlensaures Natron, und es entstehen Ätznatron und Schwefelnatrium. Außerdem enthält die Lauge neben Soda Schwefeleisennatrium, schwefligsaures, unterschwefligsaures und schwefelsaures Natron, Chlornatrium, Natriumeisencyanür und Schwefelcyannatrium u.a. Man verdampft die Lauge in Pfannen mit Oberfeuerung unter Zufluß von frischer Lauge, bis der ganze Inhalt der Pfanne in einen dicken Brei von kohlensaurem Natron mit 1 Molekül Kristallwasser verwandelt ist, und bringt diesen auf die Salzfilter, um die durch Schwefeleisen und organische Substanzen gefärbte Rotlauge, die alle Verunreinigungen und mehr Ätznatron als Soda enthält, von dem Salze zu trennen. Letzteres wird wohl mit Dampf gewaschen, die Rotlauge aber in die Pfannen zurückgepumpt oder auf Ätznatron verarbeitet. Pfannen mit Unterfeuerung liefern eine reinere Soda, nutzen aber die Wärme schlechter aus, und das ausgeschiedene Salz brennt leicht auf dem Boden fest. Letzteres wird bei der Thelenschen Pfanne vermieden, in der eine Welle mit Schaufeln rotiert, welch letztere das abgeschiedene Salz kontinuierlich an das eine Ende der Pfanne schieben, wo es ausgeschöpft wird. Die Mutterlauge wird zur Trockne verdampft, um ein Gemenge von kohlensaurem Natron und Ätznatron (kaustisches Sodasalz) zu erhalten, oder man verarbeitet sie auf Ätznatron. Soll das Ätznatron aber in Soda verwandelt werden, so versetzt man die Rotlauge mit Sägespänen, verdampft und kalziniert den Rückstand, wobei die Sägespäne zu Kohlensäure verbrennen und das Ätznatron in kohlensaures Natron, das Schwefelnatrium in schwefelsaures Natron übergeführt werden. Vollständiger wird das Schwefelnatrium oxydiert (und infolgedessen das Schwefeleisen ausgeschieden), wenn man die erwärmte Lauge in einem Koksturm einem Luftstrom entgegenführt oder ein Gemisch von Kohlensäure und Luft mittels des Körtingschen Gebläses in die Lauge bläst. Bisweilen wendet man auch Weldonschlamm (regenerierten Braunstein), der sehr kräftig oxydierend wirkt, an.
Das Rohsalz, das sich aus der verdampften Lauge ausgeschieden hat, wird im Flammofen kalziniert, um es zu entwässern, Ätznatron in kohlensaures Natron zu verwandeln, Ferrocyannatrium zu zerstören und schwefligsaures und unterschwefligsaures in schwefelsaures Natron zu verwandeln. Man benutzt zum Kalzinieren auch, namentlich bei Anwendung von Sägespänen, einen Ofen mit kreisförmigem, rotierendem Herd und mechanischem Rührapparat. Bisweilen bläut man auch die Soda durch Zusatz von etwas Ultramarin oder regeneriertem Braunstein, der blaues mangansaures Natron bildet. Das kalzinierte Sodasalz (Sekundasoda) ist weiß und soll weniger als 2 Proz. Ätznatron und weniger als 1,5 Proz. unlösliche Substanzen enthalten. Es wird in raffiniertes Sodasalz (Primasoda) verwandelt, indem man es in heißem Wasser löst, die Lösung absetzen läßt, verdampft, das ausgeschiedene Salz aussoggt, im Flammofen trocknet und glüht. Dies Salz ist ganz weiß, in Wasser vollständig löslich, frei von Eisen und Schwefelnatrium, fast frei von Ätznatron, aber von nicht höherer Gradigkeit als die Sekundasoda.
Zur Darstellung der kristallisierten Soda löst man möglichst reine Sekundasoda in heißem Wasser und bringt die geklärte Lösung in flache eiserne Kristallisiergefäße, die bis an den Rand gefüllt und mit Bandeisen bedeckt werden. Die Kristallisation beginnt an letzterm, und man erhält im Winter in 6–8, im Sommer in 14 Tagen große Kristalle, die nach oberflächlichem Abtrocknen in Fässer verpackt werden. Sie enthalten nur 0,5–1 Proz. schwefelsaures Natron und 0,3–0,4 Proz. Chlornatrium. Die Mutterlauge liefert beim Verdampfen und Kalzinieren eine besonders für die Glasfabrikation benutzte Soda. Über die Verarbeitung der Rückstände vom Auslaugen der Rohsoda s. Tafel ›Schwefelgewinnung‹.
 5. Rotierender Sodaofen.
5. Rotierender Sodaofen.Kaustische Soda (Ätznatron). Zur direkten Darstellung von Ätznatron schmilzt man Sulfat mit Kalk und Kohle, nimmt aber mehr Kohle und laugt die Rohsoda etwas heißer aus. Zur Verarbeitung von Rotlauge auf Ätznatron wird dieselbe unter Entfernung der sich ausscheidenden Salze ohne weiteres verdampft und schließlich nur das Schwefelnatrium zerstört. Soll das Ätznatron aus Rohsodalauge dargestellt werden, so muß man gebrannten Kalk in Laugen von 11–13° B. löschen, dabei rühren oder Luft einblasen, um vorhandenes Schwefelnatrium zu oxydieren. Man filtriert dann durch ein Nutschfilter aus Koks, Kies und Sand und wäscht den auf dem Filter bleibenden kohlensauren Kalk aus, der später im Sodaofen wieder verwertet werden kann. Die Lauge wird verdampft, dabei sich ausscheidendes Salz (schwefelsaures und kohlensaures Natron) entfernt, dann geklärt, wobei sich noch Chlornatrium abscheidet und nun in gußeisernen Schmelzkesseln unter Abschäumen und Entfernen der sich ausscheidenden Salze weiter erhitzt. Hat die Temperatur der Schmelze 360° erreicht, so legt man einen Deckel auf den Kessel und bläst Luft durch die Schmelze oder setzt salpetersaures Natron hinzu, um alles Schwefelnatrium zu oxydieren. Schließlich wird der abgeklärte Kesselinhalt in eiserne Tonnen (Trommeln) geschöpft.
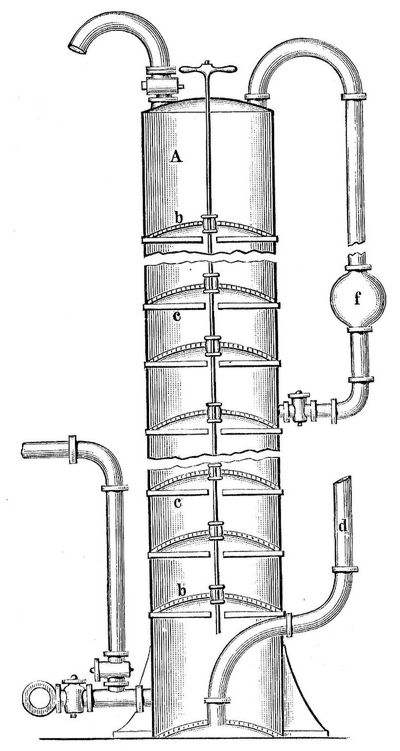
Der Ammoniaksodaprozeß beruht darauf, daß eine konzentrierte Lösung von Chlornatrium mit doppeltkohlensaurem Ammoniak einen Niederschlag von doppeltkohlensaurem Natron und eine Lösung von Chlorammonium liefert. Da also hier das Kochsalz als Lösung zur Verwendung kommt, so erspart man an Orten mit einer starken natürlichen Sole die Kosten des Versiedens. Schwache Sole verstärkt man durch Kochsalz oder Steinsalz, indem man sie systematisch durch mehrere mit Salz gefüllte Kasten fließen läßt. Etwaige Kalk- und Magnesiasalze fällt man aus der Lösung durch kohlensaures Ammoniak. Die geklärte Kochsalzlösung wird meist in Kolonnenapparaten, wie sie bei der Spiritusdestillation zur Anwendung kommen, mit Ammoniak gesättigt; sie fließt auf die oberste Terrasse und von dort abwärts durch alle Abteilungen des Apparats, während das aus Chlorammonium entwickelte Ammoniak ihr von unten nach oben entgegenströmt. Da bei der Absorption des Ammoniaks Wärme frei wird, so umgibt man den untern Teil des Apparats mit einem Mantel und kühlt mit Wasser. Das Ammoniak mindert die Löslichkeit des Chlornatriums in Wasser, man muß aber die wässerige Lösung des Salzes so stark machen, daß sie nach der Aufnahme des Ammoniaks gesättigt ist. Die Lösung fließt nun durch einen eigenartigen, automatisch wirkenden Druckkessel nach dem Karbonisationsapparat. Dieser besteht (Fig. 6) aus einem zylindrischen Turm A von 15 m Höhe, in dem fein durchlöcherte, kugelsegmentförmige Platten b und unter jeder dieser Platten ebene Platten c mit nur einem oder wenigen Löchern liegen. Während der Turm mit der ammoniakalischen Salzlösung gefüllt ist, tritt unten durch d Kohlensäure ein, die in einem Kalkofen gewonnen wird.
 6. Karbonisationsapparat von Solvay.
6. Karbonisationsapparat von Solvay.Frische Salzlösung gelangt durch das Gefäß f in den Turm, das ausgeschiedene doppeltkohlensaure Natron lagert sich auf den Platten b ab, während die Löcher in den Platten c der Lösung den Durchtritt gestatten. In regelmäßigen Zwischenräumen wird unten aus der Kolonne ein Teil der Lösung abgelassen. Bei einem andern Karbonisationsapparat sind drei schmiedeeiserne Zylinder mit konischem Unterteil zu einer Batterie vereinigt, die Kohlensäure tritt durch ein Rohr am Boden der Zylinder ein, durchströmt eine 2 m hohe Flüssigkeitsschicht und tritt dann in den zweiten und aus diesem in den dritten Zylinder. Bei der Absorption der Kohlensäure wird sehr viel Wärme frei, und man muß deshalb mit Wasser kühlen, hält aber die Temperatur auf einer gewissen Höhe, weil in der Kälte das Bikarbonat leicht durch Chlorammonium verunreinigt wird. Die aus dem Apparat austretenden Gase werden noch mit Wasser oder schwacher Sole und zuletzt mit verdünnter Schwefelsäure gewaschen, um die letzten Spuren von Ammoniak zurückzuhalten. Eine vollständige Umsetzung des Kochsalzes tritt niemals ein, vielmehr bildet sich in der Lauge ein Gleichgewichtszustand, wenn etwa zwei Drittel des Chlornatriums in Bikarbonat verwandelt sind. Das ausgeschiedene doppeltkohlensaure Natron wird auf Nutschapparaten von der Mutterlauge getrennt, durch Wasser möglichst vollständig ausgewaschen und dann in einer geschlossenen und von außen geheizten Thelenschen Pfanne in Soda verwandelt. Das in die Pfanne eingeführte Salz wird mechanisch von einem Ende derselben zum andern geschaufelt, kommt dabei an immer heißere Stellen und wird schließlich ausgeworfen. Die entwickelte Kohlensäure, die auch etwas Ammoniak enthält, saugt man mit einer Pumpe ab und benutzt sie, da sie besonders hochprozentig, zur Karbonisierung fast fertiger Lauge. Aus der von dem doppeltkohlensauren Ammoniak abgesaugten Mutterlauge, die im wesentlichen Chlorammonium enthält, und dem Waschwasser destilliert man die flüchtigen Ammoniakverbindungen ab und setzt dann Kalk zu, um auch das Ammoniak aus den nicht flüchtigen Ammoniaksalzen zu gewinnen. Als Rückstand bleibt eine Lösung von Chlorcalcium. Infolge der unvollkommenen Umsetzung des Kochsalzes erhält man beim Ammoniaksodaprozeß nur etwa 44 Proz. vom Gewicht des Kochsalzes als Soda oder 50 Proz. der theoretischen Menge, während beim Leblanc-Verfahren aus 100 kg Sulfat 150 kg Rohsoda und aus dieser 70 kg Soda von 90 Proz. (= 63 kg 100 proz. Soda) erhalten werden. Da nun 100 kg Salz 120 kg Sulfat geben, so erhält man hier aus 100 kg Salz 75,6 kg Soda oder etwa 85 Proz. der theoretischen Menge.
Bei der elektrolytischen Sodabereitung, deren Einzelheiten geheim gehalten werden, benutzt man als Kathode Eisenplatten, als Anode präparierte Kohle und trennt den Kathoden- vom Anodenraum durch eine poröse, nur für den Strom durchlässige Scheidewand aus Zement (der durch Zusatz löslicher Salze beim Gießen porös gemacht worden war), auch aus Seife etc. Den Anodenraum füllt man mit Kochsalzlösung, den Kathodenraum mit stark verdünnter Natronlauge. An der Anode scheidet sich Chlor aus, das, zu einer Flüssigkeit verdichtet, in Stahlbomben in den Handel gebracht wird, an der Kathode tritt Natrium auf, das sich im Wasser alsbald in Natriumhydroxyd (Ätznatron) verwandelt. Die Lösung wird entweder direkt eingedampft oder zur Bereitung von Soda zunächst mit Kohlensäure behandelt.
Eine ernstliche Konkurrenz droht der künstlich bereiteten Soda aus Mexiko, wo dicht an der Küste mächtige Seen entdeckt sind, aus denen Soda kristallisiert. Diese Seen sollen 75 Jahre lang täglich 100 Ton. Soda liefern können. Ist bei dieser Berechnung kalzinierte Soda gerneint, so wäre das ein Fünftel des gesamten Weltkonsums.
http://www.zeno.org/Meyers-1905. 1905–1909.
